从“神药”到天价:格列卫的救赎与拷问
01从《我不是药神》到现实:一粒药,两条命
电影散场,灯光亮起,我走出影院时天色已暗。“药给了病人活下去的希望,电影给了病人买得起药的希望”——这句观后感不是煽情,而是我对《我不是药神》最朴实的注解。银幕上,格列宁让绝症患者重燃生机;现实中,它的原型药——格列卫(Imatinib,商品名:Gleevec/Glivec)——把慢性粒细胞白血病(CML)从“绝症”拉成“慢病”。今天,让我们把镜头从银幕拉回实验室,看看这粒“神药”如何诞生,又如何站在道德与经济的十字路口。
02病与药:CML的绝境与希望
2.1 ▍ 绝境——3~5年的生存倒计时在格列卫问世前,CML几乎无药可医。标准疗法只有两条:高风险骨髓移植或干扰素+化疗。前者成功率低、风险高;后者只能把约20%~30%患者的生命延长1年。换句话说,绝大多数病人只能眼睁睁看着血象崩溃、脾脏肿大到腹部隆起,最终因感染或出血离世。
2.2 ▍ 希望——90%五年生存率的奇迹2001年格列卫上市后,多项临床追踪给出惊人数据:患者五年生存率飙升至90%左右。一粒药,把恶性血液病变成可控的慢性病,也让“慢性”二字真正落到实处。对CML患者而言,这意味着不再频繁住院、不再被“病危”通知书吓到、不再为配型骨髓而四处求人。
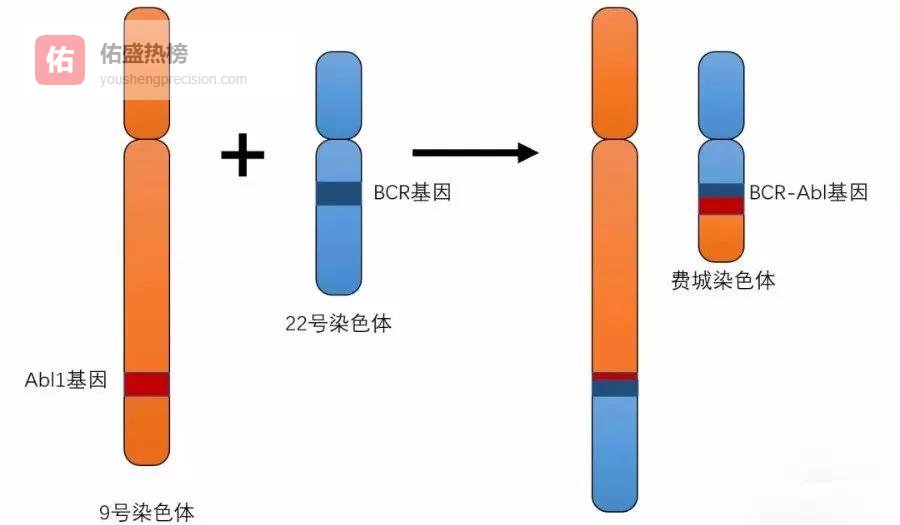
03发现之旅:从染色体易位到分子靶点
3.1 ▍ 染色体易位——癌症的“身份证”1950年代末,费城宾夕法尼亚大学病理学家Peter Nowell在显微镜下首次发现Ph染色体(现称BCR-Abl融合基因)。这一异常染色体像一枚“永不熄火的引擎”,驱动粒细胞无限增殖。CML的致病密码被破解,也为后续药物设计提供了“黄金靶点”。
3.2 ▍ 靶点锁定——STI571的意外突破1988年,俄勒冈健康与科学大学Brian Druker与瑞士化学家Nicholas Lydon联手,从炎症小分子库中筛选出化合物STI571。动物实验显示,该化合物对CML细胞株具有高度选择性杀伤,而对正常细胞几乎无影响。眼看“神药”即将诞生,却在狗身上遭遇严重肝毒性;就在项目岌岌可危时,猴子试验意外成功,让项目起死回生。
04上市前的惊魂夜:差点被“合并”掉
4.1 ▍ 公司动荡——诺华差点斩断希望正当临床申请紧锣密鼓推进时,Ciba-Geigy与另一制药巨头合并成立瑞士诺华。Lydon离任,新公司对尚未盈利的项目兴趣寥寥。格列卫一度被搁置在“冰柜”里,眼看就要胎死腹中。
4.2 ▍ 力挽狂澜——Druker说服CEO重启项目Druker锲而不舍地向诺华CEO游说,并拿出I期临床试验数据:患者总缓解率100%。数字太过耀眼,诺华高层终于松口。2001年5月,FDA破例加速审批,格列卫上市。从首次会面到FDA批准,整整耗时13年;从提交申请到获批,仅两年半。Druker与Lydon也因理性药物设计理念摘下2009年拉斯克奖。

05天价谜团:为什么穷人吃不起“救命药”?
5.1 ▍ 高价≠高成本?先算笔粗账研发成本:13年耗资数十亿美元;按2001年定价,诺华只需2年即可收回。
产能成本:原料药并非黑科技,仿制药价仅为原研的5%~10%。
失败成本:每100个项目仅1个成功,其余99个亏损由成功项目分摊。
市场规则:股价、财报、股东压力层层叠加,药企必须把利润预期写进年报。
综合来看,高定价不是实验室里的“善心”,而是资本市场里的“算术”。若研发成本无法收回,后续管线将无钱继续,更多患者将陷入“无药可用”的死循环。
5.2 ▍ 被忽视的“副作用”——全球药企裁员潮近年,国际大厂纷纷收缩研发预算:
葛兰素史克关闭张江研发中心;
诺和诺德因业绩未达标被曝全球裁员;
中国生物医药创新之城——张江、苏州、杭州——首当其冲。
当资本退潮,创新药研发从“狂欢”回到“寒冬”,“天价”与“廉价”的博弈也将更残酷地摆在患者面前。
06结语:神药仍在路上,拷问从未停歇
格列卫把CML从绝症拉成慢病,却也把“价格”推上道德法庭。它提醒我们:科技进步是一把双刃剑——既能延长生命,也能带来贫富鸿沟;既能创造商业奇迹,也可能成为利润至上的牺牲品。下一次当我们在影院为“格列宁”鼓掌时,不妨也想想实验室里那些尚未命名的分子、那些仍在排队等待骨髓移植的家庭、以及如何让更多患者吃得起那粒小小的蓝色药片。





