造物新时代:“器官”正在被打印出来!
原文发表于 《科技导报》2026年第6期《类器官生物制造研究进展及应用》
作为一种高度模拟组织器官结构与功能的体外三维(3D)模型,类器官具有重要价值。《科技导报》邀请清华大学机械工程系生物制造中心、“111 计划”生物制造与体外生命系统工程交叉学科创新引智基地、高端装备界面科学与技术全国重点实验室、组织器官生物智造与修复再生北京市重点实验室熊卓教授团队撰写文章,综述了类器官生物制造技术的研究进展。归纳了发展趋势聚焦于多工艺融合、多模态检测分析及自动化智能系统等前沿方向。梳理了类器官生物制造技术应用研究领域。针对中国现状,提出了生物材料创新、装备技术升级及推动临床转化路径的改进策略,旨在加速中国类器官生物制造技术的创新与应用。
类器官(organoids)是由多能干细胞(PSCs)、成体干细胞(ASCs)或患者来源组织(PDTs)经体外自组装形成的三维(3D)模型,可复现来源组织的空间结构、细胞多样性及关键生理功能。自2009年荷兰Hans Clevers团队利用小肠干细胞构建首个肠道类器官以来,该技术已拓展至脑、肝、肺等20余种组织模型,并于2013年被《科学》(Science)评为年度10大年度科学突破。
在组织工程和再生医学的背景下,生物制造(biofabrication)被定义为:基于细胞、生物活性分子、生物材料、细胞聚合体或细胞−材料混合物,通过生物打印或生物组装技术,结合组织成熟工艺,实现具有仿生结构和生理功能的体外模型的自动化构建。该技术不仅突破了传统类器官自组装过程的随机性局限,更从结构仿生与功能耦合2个维度推动了类器官模型的“进化”。
01
类器官的自组装构建
类器官的自组装构建是指离散细胞通过自主聚集与分化形成3D类器官的过程。
1.1 基质胶包埋法
基质胶包埋法因其对基底膜微环境的高仿生度,被视为类器官培养的“黄金标准”。其中,基质胶成分由层黏连蛋白、Ⅳ型胶原等基底膜核心组分及多种生长因子组成,可支持类器官的体外3D生长(图1(a))。然而,基质胶机械性能较弱、批次差异大且重复性低。
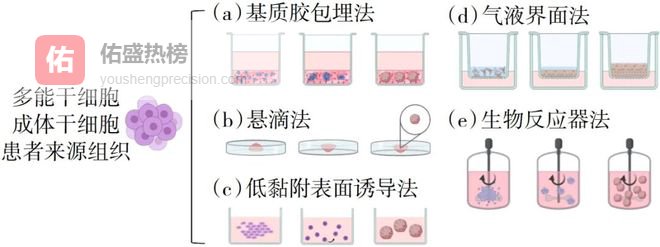
图1 类器官的自组装构建方法
1.2 悬滴法
悬滴法利用气−液界面表面张力诱导细胞自主聚集成球(图1(b)),无须外源支架即可实现3D培养,该方法已被标准化用于结直肠癌、卵巢癌等类器官的高通量构建。但受限于物理约束缺失,悬滴法类器官普遍存在结构简化问题。
1.3 低黏附表面诱导法
该技术通过聚乙二醇(PEG)修饰或微图案化处理构建低黏附表面,促使细胞自组装成簇(图1(c)),有利于干细胞生长分化,但难以控制类器官大小且营养交换效率较低,影响长期功能维持。
1.4 气液界面法
气液界面法将分离得到的组织嵌入基质胶中,底部与培养基接触,顶部则暴露于空气,从而模拟体内特定组织(如呼吸道、肿瘤微环境)的生理条件(图1(d))。然而,该方法与基质胶包埋法同样存在材料成分不确定性。
1.5 生物反应器法
生物反应器法则利用旋转容器中的动力学环境,使细胞在3D空间中均匀地生长和分化(图1(e))。该技术无需基质胶,使细胞维持悬浮状态,适合大规模类器官构建与长期培养,但该方法操作复杂且存在扩大规模时类器官均一性差的问题。
02
类器官的生物制造
类器官生物制造的核心在于对细胞微环境及细胞空间位置的精准操控,突破传统自组装培养的局限,从而实现结构精准调控与功能强化。
2.1 类器官的可控制造
类器官可控制造的技术路径可分为工程化材料介导的微环境设计、物理场驱动的生物组装和个性化的生物打印方法。
针对基质胶化学成分不明确的问题,工程化材料介导的微环境设计通过多种聚合物与化学物质赋予水凝胶所需的生化、机械和结构特性,促进类器官形成发育,为其提供更精准的生长环境。瑞士Matthias P. Lutolf团队开发了PEG杂合网络水凝胶。该团队实现了肠道类器官的局部基质软化以阐明肠道形态发生机制。而德国E. Krieg团队构建了动态DNA交联基质材料,调控类器官的发生发展。英国Molly Stevens团队采用互补凝胶网络策略实现生物材料的拓展,具有更广泛的细胞适应性。
物理场驱动的生物组装利用磁控、声场等技术进一步拓展了细胞的精确排列和组装能力。
此外,个性化的生物打印技术通过精确控制生物材料和细胞的分布,实现了类器官的个性化、功能化制造。美国郭峰团队3D打印出网状支架,将人类中脑类器官培养在支架中以模拟生理扩散特性。该工程化类器官无坏死和缺氧现象且更好地重现了药物反应。
2.2 类器官的高通量制造
目前,类器官的高通量制造技术主要包括生物3D 打印、微阵列、液滴微流控及类器官芯片技术,此类自动化方法可确保重复可靠的类器官构建,向大规模组织工程应用迈出重要一步。
澳大利亚Melissa H.Little团队将诱导性多能干细胞(iPSC)分化的肾脏祖细胞与少量培养基通过挤出式3D打印方法,构建出具有肾小球、近端小管等功能性结构的肾脏类器官(图2(a)),兼顾构建效率和稳定性。瑞士Matthias P. Lutolf团队开发出聚合物−水凝胶基质的微井阵列,实现数千个胃肠道类器官的自动化悬浮培养和实时分析(图2(b))。中国马少华团队通过液滴微流控技术将含有细胞的基质胶剪切成微球(图2(c)),结合液滴式3D打印实现了多种正常组织和肿瘤类器官的自动化快速构建。中国熊卓团队则通过液滴微流控技术高通量构建了患者来源的肺癌类组装体(assembloids),包含多种肿瘤微环境细胞的同时高度保留了源肿瘤生理特性与临床响应性(图2(d))。美国Nancy L. Allbritton团队构建出小肠类器官芯片模型(图2(e))。
因此,高通量制造的批量类器官不仅可进行药物研发,减少药物开发的时间和成本;还能够根据患者特异性反应构建出类器官模型,定制个性化治疗方案。
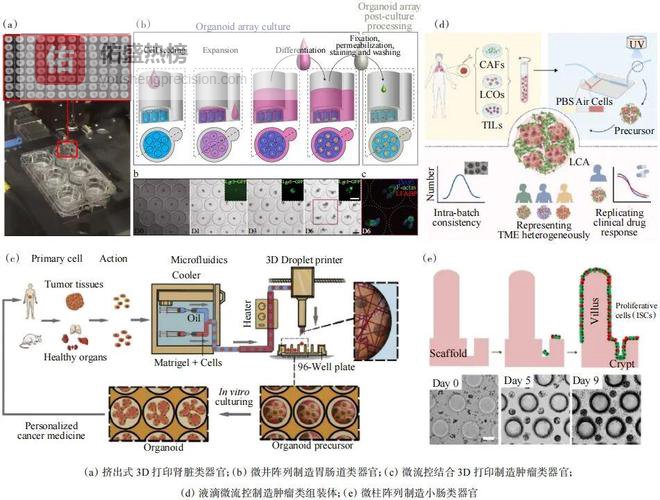
图2 类器官高通量制造方法
2.3 类器官的功能化组装
生物制造技术实现了单个类器官的可控构建和高通量制造,而功能化组装技术则是进行多个类器官的精准组装,构建具有复杂功能的大尺度组织器官。
将2个及以上的类器官在培养条件下直接组装是最简单有效的方法,美国Sergiu Pasca团队将iPSC分化培养为2类模拟不同脑区的神经类器官,使其自发融合为人类前脑组装体,从而探究功能性人脑皮质回路的发育机制。
然而,直接组装技术对空间结构的控制有限且用时较长,磁控与声控技术则可解决上述局限。美国Renata Pasqualini团队首次通过磁控将星形胶质细胞球与胶质母细胞瘤球二者组装,论证了磁控组装多类器官的可行性。美国Naside G. Durmus团队利用类器官间密度差异,通过磁控技术操纵其组装成悬浮体(levitoids),但该类技术存在潜在细胞毒性,影响后续功能性研究。声控组装技术则具有良好的细胞相容性,中国陈璞团队开发出法拉第波声学差分组装方法,构建出具有异质细胞空间排列的肝类器官模型。
可通过生物打印技术将多个类器官组装为具有特异性功能的组织器官结构,根据技术特点可分为抓放式、挤出式、悬浮式与体积式生物3D打印。抓放式打印方法,如Kenzan法和抽吸辅助法,通过物理抓取实现类器官定位。使用类器官作为生物墨水的挤出式打印方法能够更好保留类器官生理功能与结构特征。早期,美国Gabor Forgacs团队将心肌和内皮类器官装载到毛细微管中形成特定几何结构。近年来,新西兰Tim Woodfield团队借助支架结构增强了挤出式打印过程中的可控性,构建出多层软骨组织与肿瘤模型。美国Mark A. Skylar−Scott团队将全细胞墨水进行挤出式3D打印,构建出多种功能性复杂组织。而在特定研究中,微环境材料的力学性能尤为关键,因此,通常使用类器官和水凝胶材料混合物作为生物墨水挤出打印。
悬浮式打印方法拓宽了生物材料的选择范围并大幅提升了打印结构的复杂度。美国Jennifer A. Lewis团队将高密度类器官作为支撑浴,基于悬浮打印技术构建出具有可灌注血管通道的心脏组织。中国熊卓团队进一步开发出一种兼具生物墨水和支撑浴功能的双相生物墨水,实现了内外复杂结构的一体化构建。上述打印方法均通过层层堆积构建3D组织结构,而体积打印方法(VBP)则基于光固化原理,可实现极短时间内的精细结构成形。荷兰Riccardo Levato团队通过VBP将载有类器官的明胶水凝胶在20 s内成型为复杂的厘米级3D肝组织结构。
03
类器官生物制造技术趋势
3.1 多制造工艺融合
多工艺融合显著提升了类器官结构复杂性与功能仿生性。将器官芯片与微流控技术结合,可开发出集流动控制、生物物理刺激和传感器于一体的类器官培养系统;将器官芯片与多种生物3D打印技术结合,可实现功能性组织构建和动态微环境模拟与调控。此外,将液滴微流控、挤出式打印与时空组学技术结合,中国马少华团队首次在单细胞分辨率下实现了类器官结构功能的精准解析;将挤出式打印与声控技术耦合,中国陈鹭剑团队构建出类血管的环形结构和类肝小叶的蜂巢结构。
3.2 多模态检测与分析
随着传感和检测技术的持续进步,通过整合传统的光学成像技术与新兴的表征手段,多模态检测与分析技术正逐渐成为该领域的研究前沿。此类技术不仅能够捕获超越常规形态学的多层次数据,还具备对类器官3D结构的全面表征能力。
中国王平团队利用阻抗生物传感技术成功提取了嗅觉上皮类器官的生理信号(图3(a));中国蔡宗苇团队通过基质辅助激光解吸(MALDI)质谱成像技术,实现了对人气道类器官脂质组学信息的精准获取(图3(b));中国徐铭恩团队采用光学相干断层扫描(OCT)技术,快速无损地重构了类器官结构(图3(c)),获得了重要的形态学数据;美国Duygu Kuzu团队使用可植入微电极阵列,有效获取了皮质类器官的电生理信息(图3(d))。近期,拉曼光谱技术因其非侵入性、高分辨率和分子特异性等优点,在类器官的形态与成分分析、代谢物检测及发育过程评估等领域带来了新的可能性。美国闵玮团队利用相干拉曼显微镜实现了对脑类器官中神经纤维走向的观察以及肿瘤代谢活动的三维可视化。
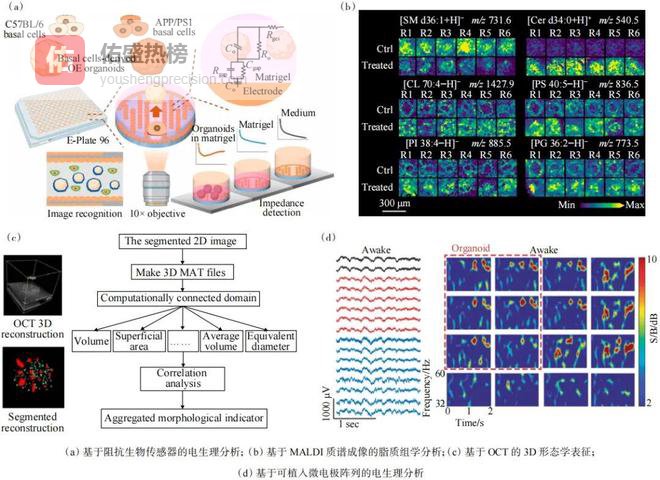
图3 类器官的多模态检测与分析
3.3 自动化智能化系统与应用
自动化系统正逐步取代传统的人工操作,不仅显著提高了实验效率,实现了大规模、快速的类器官制造与数据采集,还有效避免了人工操作引入的不稳定性因素。目前已有研究成功应用AI技术实现了对肺类器官(图4(a))和肠道类器官(图4(b))形态学特征的自动化提取。该技术还能基于提取信息,针对类器官高质量培养与临床需求进行深入分析,例如预测类器官未来分化状态以提前干预或纯化(图4(c))、开展可解释的多模态生物学分析及预测临床患者对药物的疗效(图4(d))等。
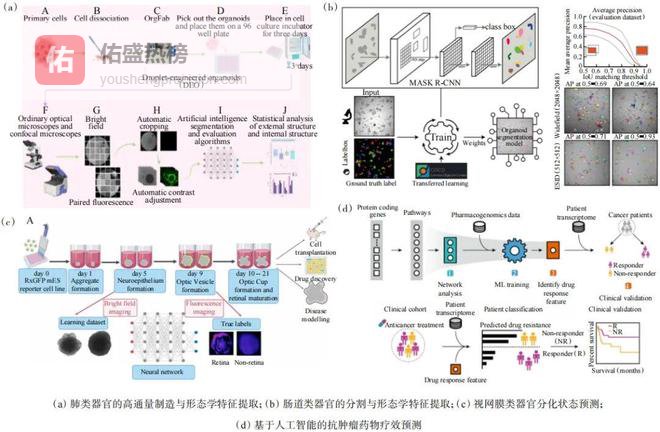
图4 基于类器官的自动化智能化系统与应用
04
类器官生物制造应用
4.1 疾病建模与机制研究
目前,脑类器官模型已被广泛用于阿尔茨海默病、帕金森病等神经退行性疾病的分子机制研究。肺泡、呼吸道及支气管类器官高通量模型也已被应用于病毒感染后机体病理改变的机制研究,筛选潜在的治疗策略。此外,通过结合CRISPR−Cas9等基因编辑技术,研究人员可以在类器官中引入或修复特定基因突变,构建高度精准的疾病模型。
4.2 再生医学与组织修复
生物制造技术可精准构建出复杂的组织结构,加速了再生医学从基础研究到临床应用的转化,为损伤组织的功能性修复提供了新的治疗手段。
4.3 个性化治疗与药物开发
类器官技术在个性化治疗与药物开发领域展现出广阔的应用价值。目前,已有36项临床试验利用类器官为患者寻找个性化肿瘤疗法,未来有望获批用于临床。随着类器官生物制造技术及AI的出现,有望在药物开发方面进行一场技术革命。AI通过机器学习和深度学习算法处理大量数据,与类器官生物制造技术结合可快速识别潜在靶点,将传统数年的过程缩短至数天或数月。
4.4 太空微重力研究应用
太空微重力环境可加速细胞衰老、改变力学信号传递及增强药物敏感性,为类器官研究提供了独特的实验平台。借助生物制造技术实现太空原位构建与培养类器官,既可规避振动损伤,又能利用微重力特性精准调控类器官发育。随着生物制造技术在太空研究中的发展,将实现太空原位构建具有复杂结构的功能化组织,为解析肌肉萎缩等重力依赖疾病机制、提出创新抗肿瘤策略提供有效平台。
05
中国类器官生物制造的发展
依托国家级干细胞资源库(如中国科学院干细胞库),中国积累了丰富的干细胞资源,为个性化类器官构建提供了原材料保障。在工程化技术研发方面,中国学者率先开发了基于丝素蛋白的生物墨水并推动了精准快速制造类器官技术应用,达到国际领先水平。此外,政策支持力度持续增强。
然而,中国类器官生物制造仍面临3大挑战:核心材料依赖进口,基质胶、合成水凝胶等关键材料国产化率低,供应链风险突出;高端装备本土化水平低,生物3D打印机、高内涵成像系统等设备仍以进口为主,制约了大规模生产;临床转化路径尚未明确,导致产业化进程滞后于欧美等国。为突破瓶颈,建议采取以下策略。
1)生物材料创新。重点开发仿生脱细胞基质材料与人工合成材料,降低对动物源基质的依赖。利用合成生物学技术构建可控降解的蛋白支架或编程细胞外基质的信号分子梯度,推动类器官发育的定向调控。力争2030年前实现核心材料国产化率超 60%。
2)装备技术升级。联合工程学科攻关,推动国产生物制造设备的精度与稳定性提升。加强与机械工程、电子工程等跨学科合作,采用高校研发、企业转化和医院验证的模式进行设备迭代。此外,建立国产生物制造设备的标准化平台,确保其可靠性和稳定性。
3)临床转化路径探索。优先推进肿瘤类器官的标准化与合规化,探索中国类器官技术标准与ISO/TC 276生物技术标准化委员会的接轨路径。同时,优化类器官临床应用的伦理审查框架,为类器官的临床转化提供伦理保障。
06
结论
类器官生物制造技术正从基础研究迈向临床转化,其核心在于借助工程化手段突破自组装局限,实现结构、功能与应用的全链条优化。生物3D打印、微流控芯片和工程化材料等技术的融合发展,提升了类器官的仿生性与可控性,并推动了高通量标准化生产。多模态检测与人工智能技术的介入,为类器官的精准分析与个性化应用提供了新的解决方案。
然而,该领域当前仍面临血管化类器官缺失、神经和免疫微环境模拟不足等瓶颈问题。未来,需通过跨学科协作,开发血管化类器官共培养系统、神经系统和免疫细胞整合技术及动态微环境调控策略。中国应充分发挥在干细胞资源和政策支持方面的优势,聚焦材料创新、装备升级与临床转化3大方向,以抢占类器官产业的制高点。
本文作者:王子萱、高洁、姬周原、周显昊、邓贺元、方永聪、熊卓
作者简介:王子萱,清华大学机械工程系生物制造中心、“111 计划”生物制造与体外生命系统工程交叉学科创新引智基地、组织器官生物智造与修复再生北京市重点实验室,博士研究生,研究方向为肿瘤体外模型的构建及应用;熊卓(通信作者),清华大学机械工程系生物制造中心、“111 计划”生物制造与体外生命系统工程交叉学科创新引智基地、高端装备界面科学与技术全国重点实验室、组织器官生物智造与修复再生北京市重点实验室,教授,研究方向为组织工程与再生医学,生物3D打印与生物制造。
文章来 源 : 王子萱, 高洁, 姬周原, 等. 类器官生物制造研究进展及应用[J]. 科技导报, 2026, 44(6): 22−34.
本文有删改,
内容为【科技导报】公众号原创,欢迎转载白名单回复后台「转载」
《科技导报》创刊于1980年,中国科协学术会刊,主要刊登科学前沿和技术热点领域突破性的研究成果、权威性的科学评论、引领性的高端综述,发表促进经济社会发展、完善科技管理、优化科研环境、培育科学文化、促进科技创新和科技成果转化的决策咨询建议。常设栏目有院士卷首语、科技新闻、科技评论、本刊专稿、特色专题、研究论文、政策建议、科技人文等。






