高中化学速查宝典:结构式、共价键到离子键一次讲透
01写在前面:一张图带你吃透“结构式”
结构式是共价化合物的“身份证”,它用短线把共用电子对“绑”在一起。记住:
只有共价化合物才有结构式
写结构式时,相邻原子必须用短线相连
未参与成键的孤对电子不能遗漏
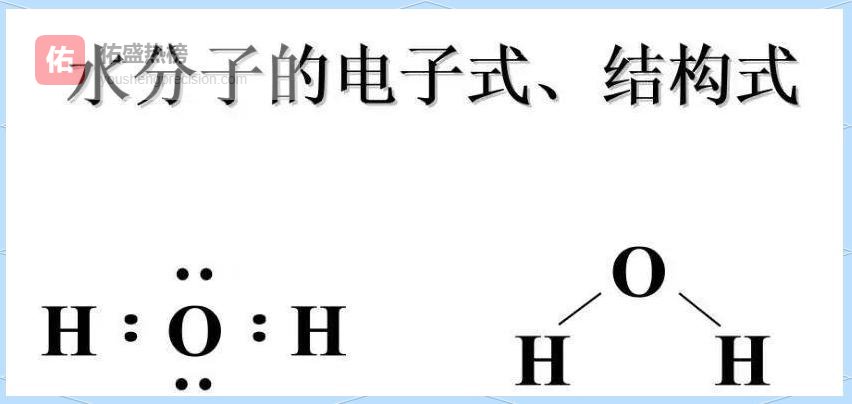
水分子的结构式就是典范:H-O-H,一目了然。


02单质与离子化合物的“身份密码”
2.1 ▲ 单质:同种元素“裸奔”的纯度证明它们没有下标,也没有离子键,电子式直接画成“·”或“×”即可。
 2.2 ▲ 离子化合物:阴阳离子“手拉手”
2.2 ▲ 离子化合物:阴阳离子“手拉手” 写电子式时,阴离子带负号,阳离子不带;若阳离子最外层电子数不是8(或2),需用方括号扩起来。
典型代表:Na₂O、MgCl₂,电子式分别如下:
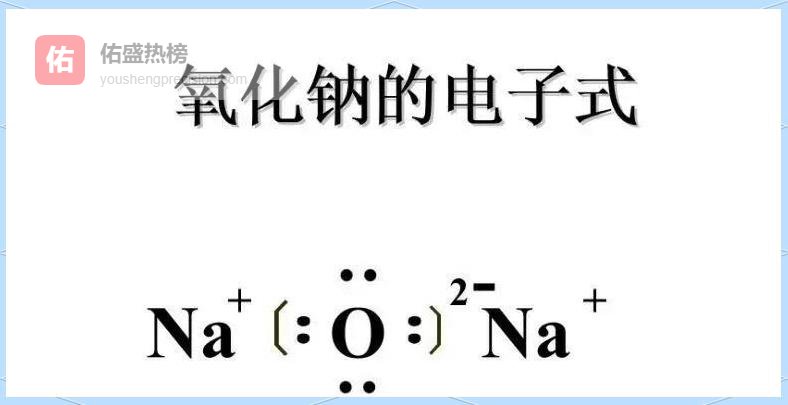

03八大类化合物速记口诀
3.1 ▲ 氧化物:O在前面就是“氧某”金属氧化物带正价,电子式先写金属再写O,中间用“·”连接
非金属氧化物带负价,O写在前面,电子式用“[]”扩住整个分子
示例:Na₂O₂、SO₃。

 3.2 ▲ 卤化物:卤素在后头
3.2 ▲ 卤化物:卤素在后头 电子式先写主族金属,再写卤素,中间加“·”,若主族金属最外层电子数=族序数,则不再重复写电子。
示例:KCl、MgBr₂。
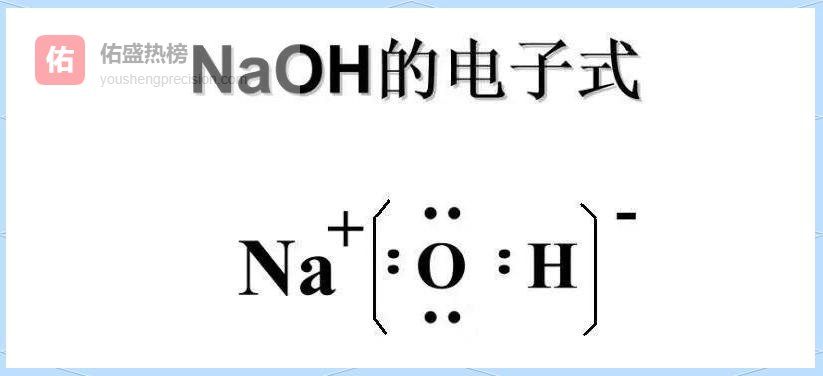
 3.3 ▲ 硫化物、氮化物、碳化物:非金属间“抱团”
3.3 ▲ 硫化物、氮化物、碳化物:非金属间“抱团” 硫化物S显-2价,写在后
氮化物N显-3价,写在后
碳化物C显-4价,写在后
规则同上,电子式只写不足电子即可。
示例:CS₂、N₂H₄、C₃N₄(石墨烯)。
 3.4 ▲ 氢化物:H永远在前头
3.4 ▲ 氢化物:H永远在前头 H的+1价被隐含在“·”里,电子式只需画出非金属元素与“·”的个数差。
示例:H₂O、NH₃。
3.5 ▲ 酸:含氧酸看“羟基”,无氧酸看“氢”含氧酸把O写在中间,H写在两端;无氧酸直接把H排成“+”即可。
示例:H₂SO₄、HCl。
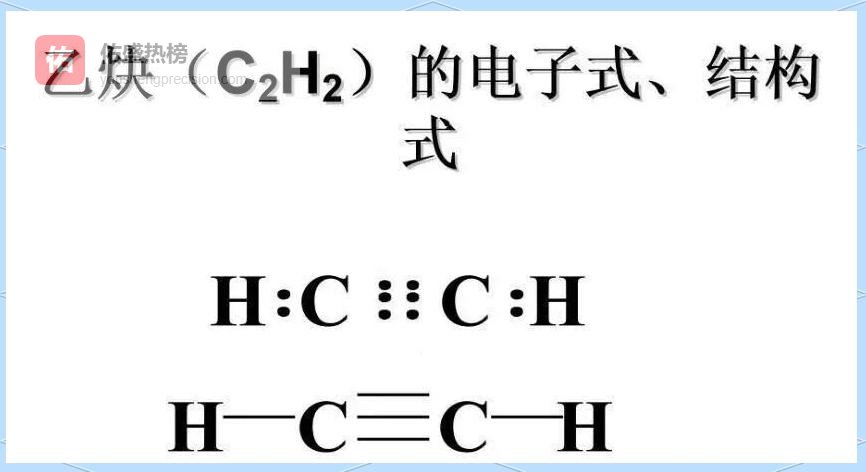
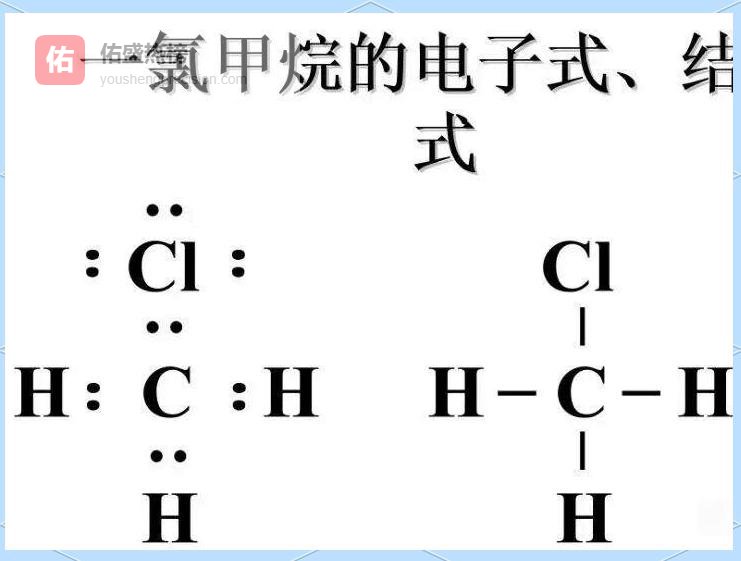
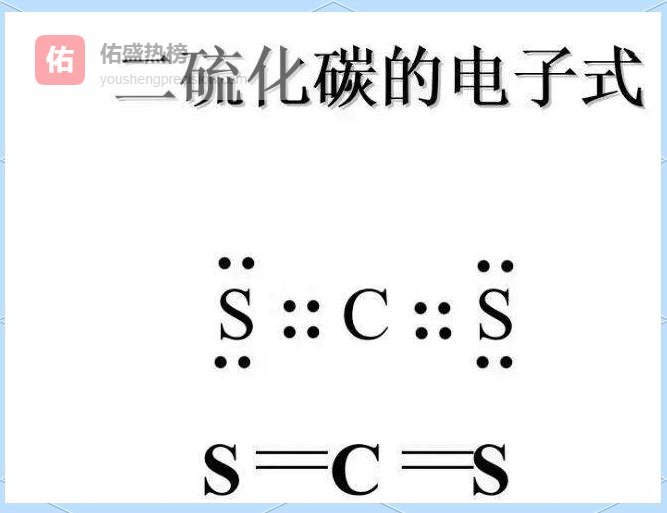 3.6 ▲ 有机物:碳链是“主干”,其余是“枝叶”
3.6 ▲ 有机物:碳链是“主干”,其余是“枝叶” 先写碳链,再写氢、氧、氮等杂原子,双键用“=”、三键用“≡”标出,孤对电子用“·”补齐。
示例:CH₃CH₂OH、CH₃COOH。
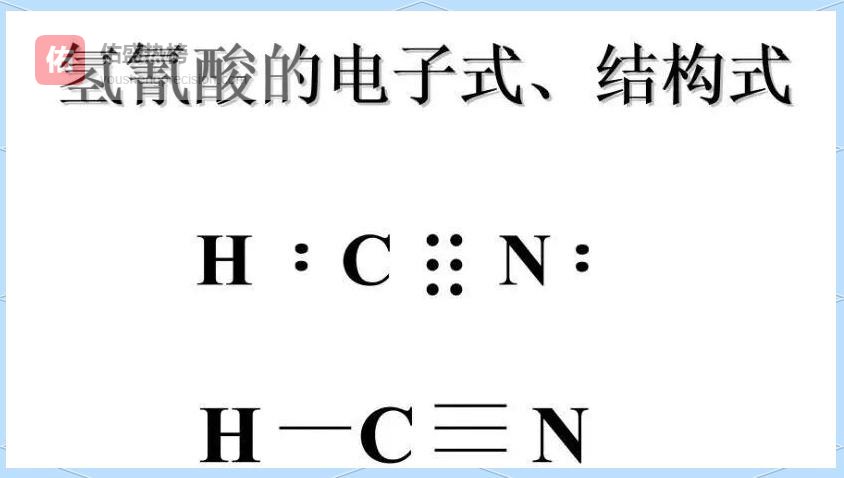
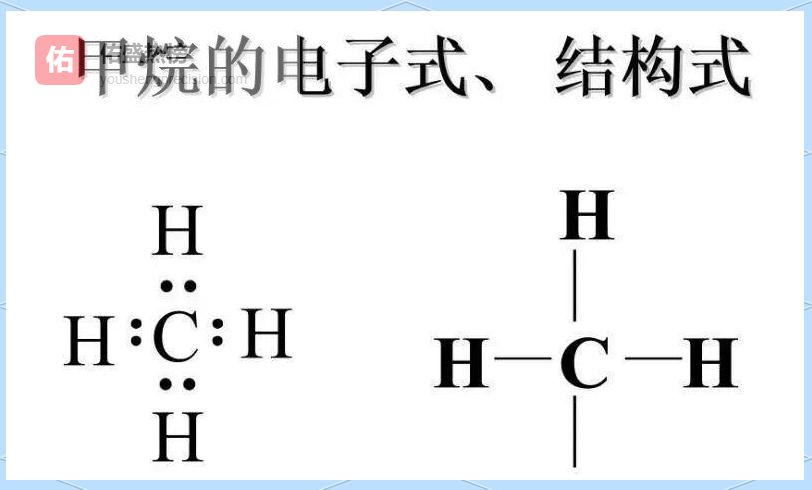
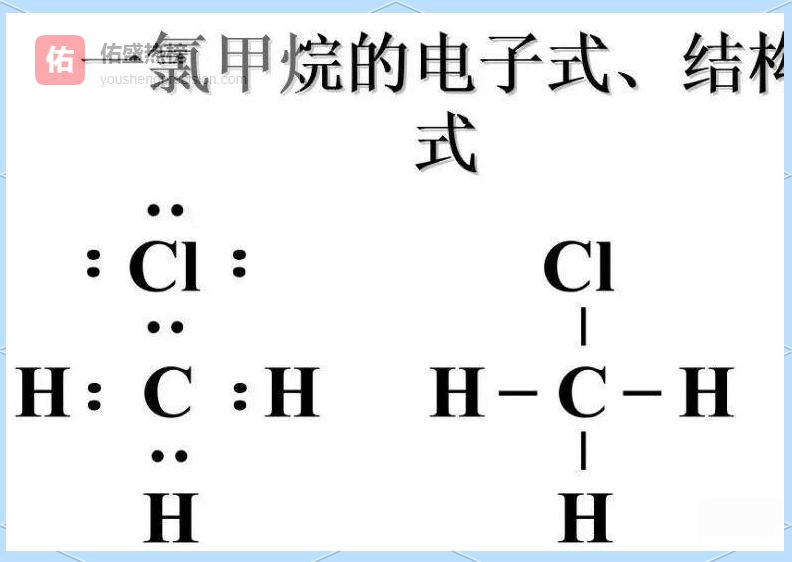
 3.7 ▲ 特殊物:叠氮化钠NaN₃
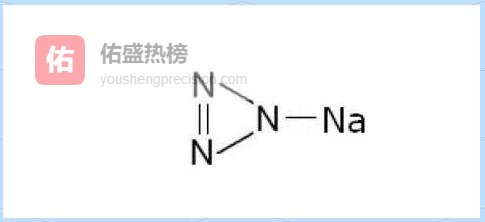
3.7 ▲ 特殊物:叠氮化钠NaN₃ N₃²⁻是等电子体,电子式把三个N排成等边三角形,中间用方括号括住,再补足8个电子即可。
示例:NaN₃。
04易错点提醒:结构式≠分子式
分子式只关心元素种类与原子个数,结构式却要求“谁和谁成键、成几对键”一目了然。
例如:CO₂与CO的结构式分别为O=C=O、C≡O,二者分子式虽同为C O₂,但结构截然不同。
牢记:结构式写错,共价键就全错。




