南开团队把“两亲”氢膦酰胺变成万能砌块
01从“两亲”到“万能”——氢膦酰胺的破局之路
膦手性化合物是药物、催化剂与先进材料的核心骨架,但其不对称合成长期被“步骤多、效率低、产物单一”三大难题困扰。传统方法依赖手性辅基拆分或非对映选择性合成,往往需要多步操作,产物结构也被严格限定。近年来,催化不对称合成虽渐成热点,却始终缺少“高选择性+高通用性”的通用方案。

02镍催化动力学拆分——99% ee的首次突破
南开大学苏波教授团队把目光投向了“两亲性”手性氢膦酰胺:分子同时带有亲核性的H-P(O)与亲电性的P–[N]结构单元,堪称理想合成砌块,却因缺乏高效手性合成路径而长期“躺平”。
团队以廉价外消旋氢膦酰胺为原料,设计镍催化动力学拆分策略,首次实现该类化合物的高对映选择性合成,ee值高达99%。这一关键突破,为后续模块化转化铺平道路。
0314类膦手性化合物“一键生成”
在手性氢膦酰胺平台分子基础上,研究团队利用P-N键与P-H键的立体专一性转化,在相同条件下分别构建了P-C、P-N、P-O、P-S等14类膦手性骨架。
P-C键——形成季碳中心,广泛存在于天然产物与药物分子
P-N键——增强分子刚性,提升光学稳定性
P-O键——引入磷氧双键,赋予材料光电性能
P-S键——提高代谢稳定性,常见于临床前候选分子
同一反应条件、同一催化剂体系,却能“一锅端”生成多样化膦手性结构,显著扩大了化学空间。
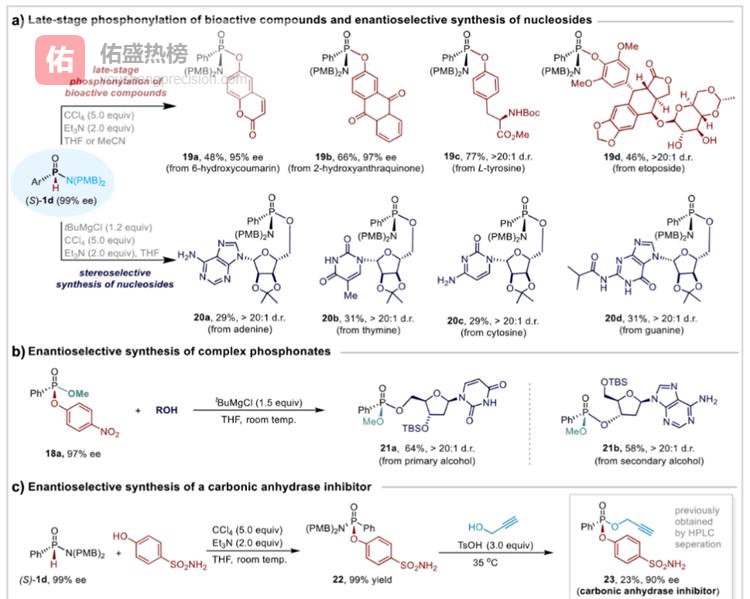
04走向药物创制——三大应用场景验证
团队进一步把通用平台推向真实药物分子:
复杂药物分子的后期膦酰化修饰——在现有药物骨架上快速引入膦手性中心,缩短改造周期
核苷类药物候选分子的不对称合成——从廉价起始原料出发,五步构建含磷核苷类似物,产率与对映选择性同步达标
手性碳酸酐酶抑制剂的快速优化——借助平台化合物的多样性,快速筛选出活性提升3倍以上的候选抑制剂
研究显示,该模块化合成策略不仅缩短了传统路线1–2步反应,还大幅降低了原料成本与操作复杂度,为“从实验室到生产线”提供了可行路径。
05写在最后
南开大学这项工作首次让“两亲”氢膦酰胺从“理想模型”变成“万能砌块”,为膦手性化合物的合成提供了“高选择性+高通用性+易操作”的全新范式。随着后续应用研究的深入,这一成果有望在药物创制、不对称催化及功能材料等多个领域催生新的突破。





