纳米战“毒”:下一代抗病毒疗法的隐形利刃
01从分子到纳米:病毒治疗的新战场
当传统抗病毒药物遭遇耐药变异、血药浓度波动或生物屏障“拒收”时,纳米级平台用尺寸优势撕开了新裂缝。它们既能作为“移动药库”精准投递,也能化身“病毒诱饵”直接阻断感染路径,为老药赋予第二春,也为新药打开设计空间。

02纳米送药:把“短命”药物变成“长跑选手”
2.1 ◇ 长循环+高载药,疏水药物也能全身遨游亲脂性抗病毒药物常因溶解度低、半衰期短而“昙花一现”。纳米颗粒把药物包进“隐形盔甲”,既保护活性分子不被酶解,又控制缓释节奏,把治疗窗口从几小时拉到数天。长循环设计减少肝脏“截胡”,高载药量则用更少量载体携带更多药物,让每一滴血浆都成为“隐形药库”。
2.2 ◇ 靶向+刺激响应,智能释放直击病灶纳米颗粒表面可“贴”上配体,像磁铁一样吸附病毒高负荷组织;同时选用pH敏感、酶敏感或温度敏感材料,在感染部位实现“可控爆破”,把药物一次性精准投放在最需要的地方,减少脱靶副作用。多价配体还能同时打开多种受体通道,提升细胞摄取效率,加速药物进入感染细胞。
03纳米诱饵:用“假想敌”阻断病毒复制
当药物难以直接对抗变异株时,“诱饵”策略成为另类破局思路。二氧化硅、金或聚合物纳米颗粒可被设计成与病毒粒子尺寸相当的“仿制外壳”,通过静电、氢键或范德华力“捕获”病毒粒子,限制其移动、融合与入侵。由于比表面积大,足够数量的纳米诱饵能在体内“网”住大量游离病毒,为免疫系统争取时间清除感染。这一机制对小分子药物难以作用的胞内阶段尤其有效。
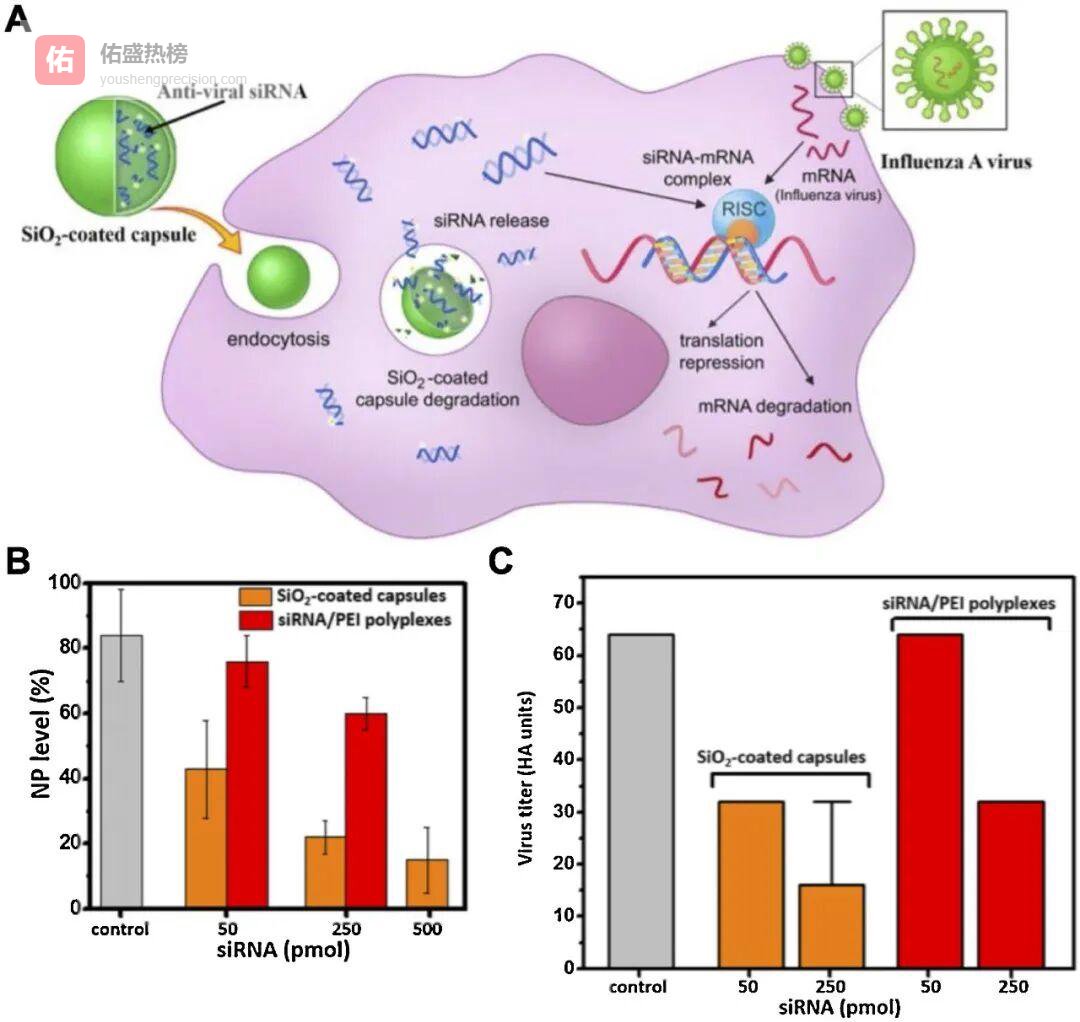 3.1 ◇ siRNA纳米胶囊:流感病毒的“基因剪刀”
3.1 ◇ siRNA纳米胶囊:流感病毒的“基因剪刀” 以流感为例,科研团队把小干扰RNA(siRNA)封装进二氧化硅微胶囊,利用细胞内吞途径把RNA释放到胞质中,与RNA诱导沉默复合体(RISC)结合,特异性剪切病毒mRNA,从而阻断核蛋白(NP)表达。实验显示,经微胶囊处理的A549细胞上清液中H1N1病毒滴度显著下降,证明纳米载体能把基因沉默疗法安全送进呼吸道细胞。
04未来展望:从应急工具到常态防控
随着脂质体、聚合物与无机纳米粒的定制精度不断提升,抗病毒治疗正从“一刀切”走向精准医疗。纳米技术不仅能克服耐药、血药浓度与生物屏障三大痛点,还为个性化疫苗、肿瘤病毒联合疗法甚至病原体监测传感器提供了一体化平台。当新型病毒再次来袭,这套“纳米防线”或许能比传统手段更快地给出解药。





